De maximale hoeveelheid van een opgeloste stof opgelost in een oplosmiddel bij evenwicht wordt beschreven als oplosbaarheid. Een onoplosbare verbinding is een verbinding die een neerslag (een kristallijne of amorfe vaste stof) in de oplossing zal vormen. Het kan gedeeltelijk oplosbaar zijn, maar is onoplosbaar gelabeld voor de doeleinden van de chemie.[1] Het onthouden van de oplosbaarheidsregels zal uw leven een stuk eenvoudiger maken wanneer u met de chemische vergelijkingen werkt. Met wat tijd, moeite en een paar geheugentrucs, heb je alle regels in een mum van tijd opgeslagen.
Methode één van de drie:
De oplosbaarheidsregels leren
-
 1 Erken dat zouten die groep IA-elementen bevatten oplosbaar zijn. Het periodieke systeem is ingedeeld in rijen en kolommen die respectievelijk periodes en groepen worden genoemd. De eerste kolom van de tabel bevat de elementen van groep 1A. Het zijn de alkalimetalen en omvatten Li, Na, K, Cs en Rb.[2]
1 Erken dat zouten die groep IA-elementen bevatten oplosbaar zijn. Het periodieke systeem is ingedeeld in rijen en kolommen die respectievelijk periodes en groepen worden genoemd. De eerste kolom van de tabel bevat de elementen van groep 1A. Het zijn de alkalimetalen en omvatten Li, Na, K, Cs en Rb.[2] - Bijvoorbeeld: KCl en LiOH zijn oplosbaar in water.[3]
-
 2 Weet dat zouten die nitraten, chloraten en acetaten bevatten oplosbaar zijn. Wanneer een nitraat, NO3-, chloraat, ClO3-of acetaat, CH3COO-, vormen een zout, ze zijn oplosbaar in water.[4]
2 Weet dat zouten die nitraten, chloraten en acetaten bevatten oplosbaar zijn. Wanneer een nitraat, NO3-, chloraat, ClO3-of acetaat, CH3COO-, vormen een zout, ze zijn oplosbaar in water.[4] - Bijvoorbeeld: KNO3, NaClO3en CH3COONa zijn allemaal oplosbaar.[5]
-
 3 Begrijp dat alle ammoniumzouten oplosbaar zijn. Het ammoniumion, NH4+, maakt zoutverbindingen die volledig dissociëren in aanwezigheid van water. Er zijn geen uitzonderingen op deze regel.[6]
3 Begrijp dat alle ammoniumzouten oplosbaar zijn. Het ammoniumion, NH4+, maakt zoutverbindingen die volledig dissociëren in aanwezigheid van water. Er zijn geen uitzonderingen op deze regel.[6] - Bijvoorbeeld: NH4OH is oplosbaar hoewel het een hydroxide bevat.
-
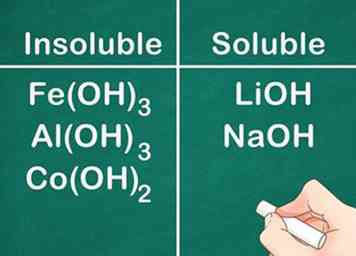 4 Weet dat de meeste hydroxideverbindingen onoplosbaar zijn. Sommige hydroxidezouten zijn enigszins oplosbaar: hydroxiden gevormd met Groep 2-elementen (Ca, Sr en Ba). De uitzondering op deze regel is dat hydroxidezouten gevormd met Groep 1-elementen oplosbaar zijn omdat Groep IA-elementen altijd oplosbaar zijn.[7]
4 Weet dat de meeste hydroxideverbindingen onoplosbaar zijn. Sommige hydroxidezouten zijn enigszins oplosbaar: hydroxiden gevormd met Groep 2-elementen (Ca, Sr en Ba). De uitzondering op deze regel is dat hydroxidezouten gevormd met Groep 1-elementen oplosbaar zijn omdat Groep IA-elementen altijd oplosbaar zijn.[7] - Bijvoorbeeld: Fe (OH)3, Al (OH)3en Co (OH)2 onoplosbaar, maar LiOH en NaOH zijn oplosbaar.
-
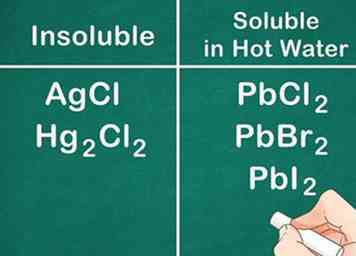 5 Erken dat zouten die niet-metalen uit Groep 17 bevatten in het algemeen oplosbaar zijn. Groep 17 niet-metalen omvatten chloor (Cl-), broom (Br-) en jodium (I.-). Uitzonderingen op deze regel zijn zilver, lood en kwik. Verbindingen die bestaan uit deze niet-metalen en ionen, halide-zouten genaamd, zijn niet oplosbaar.[8]
5 Erken dat zouten die niet-metalen uit Groep 17 bevatten in het algemeen oplosbaar zijn. Groep 17 niet-metalen omvatten chloor (Cl-), broom (Br-) en jodium (I.-). Uitzonderingen op deze regel zijn zilver, lood en kwik. Verbindingen die bestaan uit deze niet-metalen en ionen, halide-zouten genaamd, zijn niet oplosbaar.[8] - Bijvoorbeeld: AgCl en Hg2cl2 zijn beide onoplosbaar.
- Merk op dat PbCl2, PbBr2en PbI2 zijn oplosbaar in HEET water.[9]
-
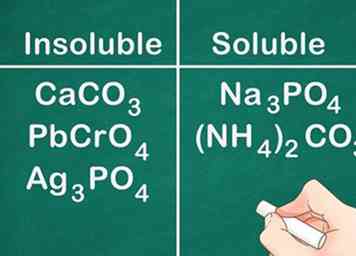 6 Weet dat de meeste carbonaten, chromaten en fosfaten onoplosbaar zijn. De chemische formules voor elk van deze zijn als volgt: CO3 (carbonaten), CrO4 (chromaten) en PO4 (Fosfaten). Uitzonderingen op deze regel zijn de metalen uit Groep 1A en NH4+ verbindingen die oplosbaar zijn.
6 Weet dat de meeste carbonaten, chromaten en fosfaten onoplosbaar zijn. De chemische formules voor elk van deze zijn als volgt: CO3 (carbonaten), CrO4 (chromaten) en PO4 (Fosfaten). Uitzonderingen op deze regel zijn de metalen uit Groep 1A en NH4+ verbindingen die oplosbaar zijn. - Bijvoorbeeld: verbindingen zoals CaCO3, PbCrO4en Ag3PO4 zijn allemaal onoplosbaar terwijl verbindingen zoals Na3PO4 en (NH4)2CO3 zijn oplosbaar.
-
 7 Begrijp dat de meeste sulfaatzouten oplosbaar zijn. De meeste zoutverbindingen die SO bevatten4 zijn oplosbaar in water. Uitzonderingen op deze regel zijn de volgende ionen Ca+2, Ba+2, Pb+2, Ag+, Sr+2en Hg+2. Sulfaatzouten die deze ionen bevatten zijn onoplosbaar.[10]
7 Begrijp dat de meeste sulfaatzouten oplosbaar zijn. De meeste zoutverbindingen die SO bevatten4 zijn oplosbaar in water. Uitzonderingen op deze regel zijn de volgende ionen Ca+2, Ba+2, Pb+2, Ag+, Sr+2en Hg+2. Sulfaatzouten die deze ionen bevatten zijn onoplosbaar.[10] - Bijvoorbeeld: Na2ZO4 is volledig oplosbaar, maar CaSO4 en BaSO4 zijn niet oplosbaar.[11]
-
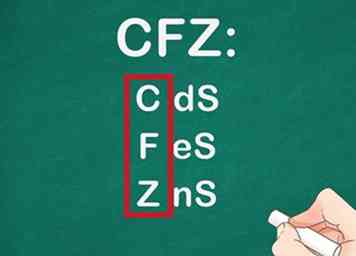
 8 Erken dat de meeste sulfiden onoplosbaar zijn in water. Zoals met veel van de andere regels, zijn er uitzonderingen, waaronder barium, calcium, magnesium, natrium, kalium en ammonium. Alleen sulfideverbindingen gemaakt met deze elementen zijn oplosbaar in water.[12]
8 Erken dat de meeste sulfiden onoplosbaar zijn in water. Zoals met veel van de andere regels, zijn er uitzonderingen, waaronder barium, calcium, magnesium, natrium, kalium en ammonium. Alleen sulfideverbindingen gemaakt met deze elementen zijn oplosbaar in water.[12] - Bijvoorbeeld: CdS, FeS en ZnS zijn allemaal onoplosbaar.[13]
- Aan de andere kant zijn sulfiden van overgangsmetalen zeer onoplosbaar.
Methode twee van drie:
Het gebruik van de NAG SAG Mnemonic
-
 1 Gebruik de mnemonic NAG SAG. NAG SAG is een gemakkelijke manier om de oplosbare verbindingen en de uitzonderingen op oplosbaarheid te onthouden. Schrijf NAG SAG op als een acrostichon en onthoud waar elke letter voor staat.[14] Hoewel dit ezelsbruggetje niet alle oplosbaarheidsregels bevat, dekt het er veel van. Alle letters vertegenwoordigen oplosbare moleculen.
1 Gebruik de mnemonic NAG SAG. NAG SAG is een gemakkelijke manier om de oplosbare verbindingen en de uitzonderingen op oplosbaarheid te onthouden. Schrijf NAG SAG op als een acrostichon en onthoud waar elke letter voor staat.[14] Hoewel dit ezelsbruggetje niet alle oplosbaarheidsregels bevat, dekt het er veel van. Alle letters vertegenwoordigen oplosbare moleculen. - N: Nitraten (NO3-)
- A: Acetaten (CH3COO-)
- G: Groep 1 alkalimetalen (Li+, Na+, enz)
- S: Sulfaten (SO4-2)
- A: Ammoniumionen (NH4+)
- G: Groep 17 niet-metalen (F-, Cl-, Br-, Ik-, enz.)
-
 2 Schrijf PMS om de eerste uitzondering te vertegenwoordigen. P staat voor Pb+2 (lood). M staat voor Mercury (Hg2+2). S staat voor Silver (Ag+). Deze 3 ionen zijn nooit oplosbaar met de sulfaatgroep of groep 17 niet-metalen.[15]
2 Schrijf PMS om de eerste uitzondering te vertegenwoordigen. P staat voor Pb+2 (lood). M staat voor Mercury (Hg2+2). S staat voor Silver (Ag+). Deze 3 ionen zijn nooit oplosbaar met de sulfaatgroep of groep 17 niet-metalen.[15] - Wanneer je het geheugensteuntje schrijft, plaats dan een ster naast PMS en een vergelijkbare ster naast de S en G van SAG om te onthouden dat dit uitzonderingen zijn.
-
 3 Onthoud Castro Bear om de tweede uitzondering te vertegenwoordigen. Castro Bear klinkt misschien gek, maar het staat voor de 3 ionen Calcium (Ca+2), Strontium (Sr+2) en Barium (Ba+2). Deze 3 ionen zijn nooit oplosbaar met sulfaten.[16]
3 Onthoud Castro Bear om de tweede uitzondering te vertegenwoordigen. Castro Bear klinkt misschien gek, maar het staat voor de 3 ionen Calcium (Ca+2), Strontium (Sr+2) en Barium (Ba+2). Deze 3 ionen zijn nooit oplosbaar met sulfaten.[16] - Bij het schrijven van de mnemonic, zet een kruis naast Castro Bear en een ander kruis naast de S in SAG om te onthouden dat deze ionen uitzonderingen zijn op de sulfaatoplosbaarheid.
Methode drie van drie:
De basisbeginselen onthouden
-
 1 Beoordeel het materiaal regelmatig. Alles opslaan kost tijd en moeite. Hoe vaker u het materiaal ziet, hoe groter de kans dat u het later onthoudt. Lees de regels vaak door en ondervraag ze dagelijks.
1 Beoordeel het materiaal regelmatig. Alles opslaan kost tijd en moeite. Hoe vaker u het materiaal ziet, hoe groter de kans dat u het later onthoudt. Lees de regels vaak door en ondervraag ze dagelijks. - Vraag vrienden en familie om u tijdens de lunch of tijdens het diner te ondervragen over de oplosbaarheidsregels.
- Houd een kopie van de regels bij de hand om te zien of u wat downtime hebt.
-
 2 Maak en gebruik flashcards. Flashcards zijn een geweldige manier om snel veel materiaal te beoordelen en te onthouden.[17] Maak flashcards met de oplosbaarheidsregels erop en enkele voorbeeldsamenstellingen. Ga door de kaarten totdat je de regels kent en welke verbindingen oplosbaar zijn of niet.
2 Maak en gebruik flashcards. Flashcards zijn een geweldige manier om snel veel materiaal te beoordelen en te onthouden.[17] Maak flashcards met de oplosbaarheidsregels erop en enkele voorbeeldsamenstellingen. Ga door de kaarten totdat je de regels kent en welke verbindingen oplosbaar zijn of niet. - Neem je flashcards mee en haal ze uit als je in de auto zit of op vrienden wacht.
- Elke hoeveelheid downtime is goed voor het beoordelen van flashcards.
-
 3 Gebruik mnemonics. Mnemonics zijn speciale geheugentrucs waarmee u informatie snel en gemakkelijk kunt memoriseren.[18] Bij het leren van een ezelsbruggetje is het handig om het meerdere keren op te schrijven totdat je het kunt onthouden. Het geheugensteuntje is alleen nuttig als je weet waar alles voor staat!
3 Gebruik mnemonics. Mnemonics zijn speciale geheugentrucs waarmee u informatie snel en gemakkelijk kunt memoriseren.[18] Bij het leren van een ezelsbruggetje is het handig om het meerdere keren op te schrijven totdat je het kunt onthouden. Het geheugensteuntje is alleen nuttig als je weet waar alles voor staat! - Vaak oefen het opschrijven van de mnemonic en waar elke letter voor staat, zodat je niet vergeet.
- Wanneer u een test of quiz krijgt, noteer eerst het ezelsbruggetje, zodat u er de rest van de tijd naar kunt verwijzen.
Facebook
Twitter
Google+
 Minotauromaquia
Minotauromaquia
 1 Erken dat zouten die groep IA-elementen bevatten oplosbaar zijn. Het periodieke systeem is ingedeeld in rijen en kolommen die respectievelijk periodes en groepen worden genoemd. De eerste kolom van de tabel bevat de elementen van groep 1A. Het zijn de alkalimetalen en omvatten Li, Na, K, Cs en Rb.[2]
1 Erken dat zouten die groep IA-elementen bevatten oplosbaar zijn. Het periodieke systeem is ingedeeld in rijen en kolommen die respectievelijk periodes en groepen worden genoemd. De eerste kolom van de tabel bevat de elementen van groep 1A. Het zijn de alkalimetalen en omvatten Li, Na, K, Cs en Rb.[2]  2 Weet dat zouten die nitraten, chloraten en acetaten bevatten oplosbaar zijn. Wanneer een nitraat, NO3-, chloraat, ClO3-of acetaat, CH3COO-, vormen een zout, ze zijn oplosbaar in water.[4]
2 Weet dat zouten die nitraten, chloraten en acetaten bevatten oplosbaar zijn. Wanneer een nitraat, NO3-, chloraat, ClO3-of acetaat, CH3COO-, vormen een zout, ze zijn oplosbaar in water.[4]  3 Begrijp dat alle ammoniumzouten oplosbaar zijn. Het ammoniumion, NH4+, maakt zoutverbindingen die volledig dissociëren in aanwezigheid van water. Er zijn geen uitzonderingen op deze regel.[6]
3 Begrijp dat alle ammoniumzouten oplosbaar zijn. Het ammoniumion, NH4+, maakt zoutverbindingen die volledig dissociëren in aanwezigheid van water. Er zijn geen uitzonderingen op deze regel.[6] 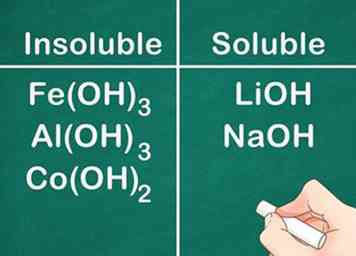 4 Weet dat de meeste hydroxideverbindingen onoplosbaar zijn. Sommige hydroxidezouten zijn enigszins oplosbaar: hydroxiden gevormd met Groep 2-elementen (Ca, Sr en Ba). De uitzondering op deze regel is dat hydroxidezouten gevormd met Groep 1-elementen oplosbaar zijn omdat Groep IA-elementen altijd oplosbaar zijn.[7]
4 Weet dat de meeste hydroxideverbindingen onoplosbaar zijn. Sommige hydroxidezouten zijn enigszins oplosbaar: hydroxiden gevormd met Groep 2-elementen (Ca, Sr en Ba). De uitzondering op deze regel is dat hydroxidezouten gevormd met Groep 1-elementen oplosbaar zijn omdat Groep IA-elementen altijd oplosbaar zijn.[7] 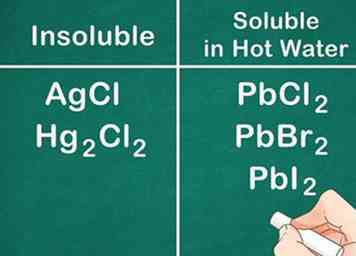 5 Erken dat zouten die niet-metalen uit Groep 17 bevatten in het algemeen oplosbaar zijn. Groep 17 niet-metalen omvatten chloor (Cl-), broom (Br-) en jodium (I.-). Uitzonderingen op deze regel zijn zilver, lood en kwik. Verbindingen die bestaan uit deze niet-metalen en ionen, halide-zouten genaamd, zijn niet oplosbaar.[8]
5 Erken dat zouten die niet-metalen uit Groep 17 bevatten in het algemeen oplosbaar zijn. Groep 17 niet-metalen omvatten chloor (Cl-), broom (Br-) en jodium (I.-). Uitzonderingen op deze regel zijn zilver, lood en kwik. Verbindingen die bestaan uit deze niet-metalen en ionen, halide-zouten genaamd, zijn niet oplosbaar.[8] 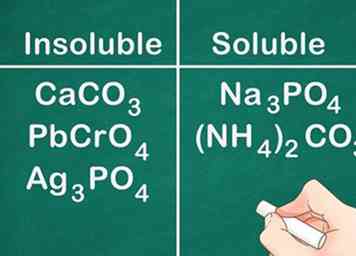 6 Weet dat de meeste carbonaten, chromaten en fosfaten onoplosbaar zijn. De chemische formules voor elk van deze zijn als volgt: CO3 (carbonaten), CrO4 (chromaten) en PO4 (Fosfaten). Uitzonderingen op deze regel zijn de metalen uit Groep 1A en NH4+ verbindingen die oplosbaar zijn.
6 Weet dat de meeste carbonaten, chromaten en fosfaten onoplosbaar zijn. De chemische formules voor elk van deze zijn als volgt: CO3 (carbonaten), CrO4 (chromaten) en PO4 (Fosfaten). Uitzonderingen op deze regel zijn de metalen uit Groep 1A en NH4+ verbindingen die oplosbaar zijn.  7 Begrijp dat de meeste sulfaatzouten oplosbaar zijn. De meeste zoutverbindingen die SO bevatten4 zijn oplosbaar in water. Uitzonderingen op deze regel zijn de volgende ionen Ca+2, Ba+2, Pb+2, Ag+, Sr+2en Hg+2. Sulfaatzouten die deze ionen bevatten zijn onoplosbaar.[10]
7 Begrijp dat de meeste sulfaatzouten oplosbaar zijn. De meeste zoutverbindingen die SO bevatten4 zijn oplosbaar in water. Uitzonderingen op deze regel zijn de volgende ionen Ca+2, Ba+2, Pb+2, Ag+, Sr+2en Hg+2. Sulfaatzouten die deze ionen bevatten zijn onoplosbaar.[10]  8 Erken dat de meeste sulfiden onoplosbaar zijn in water. Zoals met veel van de andere regels, zijn er uitzonderingen, waaronder barium, calcium, magnesium, natrium, kalium en ammonium. Alleen sulfideverbindingen gemaakt met deze elementen zijn oplosbaar in water.[12]
8 Erken dat de meeste sulfiden onoplosbaar zijn in water. Zoals met veel van de andere regels, zijn er uitzonderingen, waaronder barium, calcium, magnesium, natrium, kalium en ammonium. Alleen sulfideverbindingen gemaakt met deze elementen zijn oplosbaar in water.[12]  1 Gebruik de mnemonic NAG SAG. NAG SAG is een gemakkelijke manier om de oplosbare verbindingen en de uitzonderingen op oplosbaarheid te onthouden. Schrijf NAG SAG op als een acrostichon en onthoud waar elke letter voor staat.[14] Hoewel dit ezelsbruggetje niet alle oplosbaarheidsregels bevat, dekt het er veel van. Alle letters vertegenwoordigen oplosbare moleculen.
1 Gebruik de mnemonic NAG SAG. NAG SAG is een gemakkelijke manier om de oplosbare verbindingen en de uitzonderingen op oplosbaarheid te onthouden. Schrijf NAG SAG op als een acrostichon en onthoud waar elke letter voor staat.[14] Hoewel dit ezelsbruggetje niet alle oplosbaarheidsregels bevat, dekt het er veel van. Alle letters vertegenwoordigen oplosbare moleculen.  2 Schrijf PMS om de eerste uitzondering te vertegenwoordigen. P staat voor Pb+2 (lood). M staat voor Mercury (Hg2+2). S staat voor Silver (Ag+). Deze 3 ionen zijn nooit oplosbaar met de sulfaatgroep of groep 17 niet-metalen.[15]
2 Schrijf PMS om de eerste uitzondering te vertegenwoordigen. P staat voor Pb+2 (lood). M staat voor Mercury (Hg2+2). S staat voor Silver (Ag+). Deze 3 ionen zijn nooit oplosbaar met de sulfaatgroep of groep 17 niet-metalen.[15]  3 Onthoud Castro Bear om de tweede uitzondering te vertegenwoordigen. Castro Bear klinkt misschien gek, maar het staat voor de 3 ionen Calcium (Ca+2), Strontium (Sr+2) en Barium (Ba+2). Deze 3 ionen zijn nooit oplosbaar met sulfaten.[16]
3 Onthoud Castro Bear om de tweede uitzondering te vertegenwoordigen. Castro Bear klinkt misschien gek, maar het staat voor de 3 ionen Calcium (Ca+2), Strontium (Sr+2) en Barium (Ba+2). Deze 3 ionen zijn nooit oplosbaar met sulfaten.[16]  1 Beoordeel het materiaal regelmatig. Alles opslaan kost tijd en moeite. Hoe vaker u het materiaal ziet, hoe groter de kans dat u het later onthoudt. Lees de regels vaak door en ondervraag ze dagelijks.
1 Beoordeel het materiaal regelmatig. Alles opslaan kost tijd en moeite. Hoe vaker u het materiaal ziet, hoe groter de kans dat u het later onthoudt. Lees de regels vaak door en ondervraag ze dagelijks.  2 Maak en gebruik flashcards. Flashcards zijn een geweldige manier om snel veel materiaal te beoordelen en te onthouden.[17] Maak flashcards met de oplosbaarheidsregels erop en enkele voorbeeldsamenstellingen. Ga door de kaarten totdat je de regels kent en welke verbindingen oplosbaar zijn of niet.
2 Maak en gebruik flashcards. Flashcards zijn een geweldige manier om snel veel materiaal te beoordelen en te onthouden.[17] Maak flashcards met de oplosbaarheidsregels erop en enkele voorbeeldsamenstellingen. Ga door de kaarten totdat je de regels kent en welke verbindingen oplosbaar zijn of niet.  3 Gebruik mnemonics. Mnemonics zijn speciale geheugentrucs waarmee u informatie snel en gemakkelijk kunt memoriseren.[18] Bij het leren van een ezelsbruggetje is het handig om het meerdere keren op te schrijven totdat je het kunt onthouden. Het geheugensteuntje is alleen nuttig als je weet waar alles voor staat!
3 Gebruik mnemonics. Mnemonics zijn speciale geheugentrucs waarmee u informatie snel en gemakkelijk kunt memoriseren.[18] Bij het leren van een ezelsbruggetje is het handig om het meerdere keren op te schrijven totdat je het kunt onthouden. Het geheugensteuntje is alleen nuttig als je weet waar alles voor staat!